連載「博士のホップノート」|第1章 ホップの苦味の科学
第1章 ホップの苦味の科学
ホップには「α酸」と呼ばれる成分があります。アルファ(α)があるなら、その次のベータ(β)もあるのですが、まずはこのα酸についてお話ししましょう。
はじめにα酸あり!
α酸は、専門的には「diprenylated derivative of phloroglucinol」(Biendlら、2014)とされるもので、六角形の環状構造に2本の側鎖が伸びたような形をしています(構造式は後ほど示します)。
α酸は、ホップ(Humulus lupulus L.)でのみ確認されている物質であり、野生種のホップからも検出されています。一方で、ホップの近縁種であるカナムグラ(Humulus japonicus L.)ではその存在が報告されていないため、Humulus「属」全体ではなく、Humulus lupulus L.という「種」固有の成分であると考えられます。
このα酸こそが、ビールをビールたらしめる重要な成分です。決して大げさな表現ではないことを、これからホップとα酸の詳細を説明しながら確認していきましょう。
「ホップ」という名称は、一般的に、Humulus lupulus L.の雌株に形成される花序、すなわち毬花(きゅうか:ノート1)を指します。毬花は、花びらのように見える「苞(ほう)」と、その付け根にあたる「中軸」から構成されています。苞はさらに「外苞」と「内苞」に分かれ、横に並ぶ2枚の内苞を1枚の外苞が上から包むように、秩序立って配置されています。
内苞の付け根には、受粉が成立すれば種子が内苞に抱かれるように形成されます。そして、種子を包む部分(一般的な栽培ホップは未受精のままですが)に、ルプリンと呼ばれる分泌物を貯める器官が、毬花の成長とともに現れます。
ルプリンは直径0.15~0.20mmほどの顆粒状の構造で、その内部にはビールに欠かせない成分――α酸などの苦味成分や香り成分――が蓄えられています。
ルプリンは、はじめに杯状に細胞が配列し、そこから成分が分泌されます。これらの細胞は、外部環境への直接的な露出を防ぐために、多糖やワックス(炭化水素)から成るクチクラ層に覆われています。分泌された成分は、このクチクラ層と細胞との間に徐々に蓄積され、最終的には顆粒がパンパンに膨れ上がるかたちになります。
ルプリンは葉の裏側にもわずかに形成されますが、圧倒的に多くは毬花、しかも内苞の部分に集中して形成されます。これは、特定の器官にのみ着生する「組織局在性」を示しており、ホップという植物にとって何らかの意味があるように思えてなりません。
ルプリン内に分泌される成分、すなわちα酸などの苦味成分は、水に溶けにくい樹脂成分です。香り成分は、別名「エッセンシャルオイル」と呼ばれる油性成分であり、やはり水には溶けにくい性質を持っています。
これらの成分は、炭素数が少なく水に溶けやすい小さな分子をもとに、酵素の働きによって徐々に大きな分子へと合成されていきます。その過程で、性質も水溶性から難水溶性へと変化していきます。
一般に、細胞内は中性かつ水溶性の環境に保たれているため、水に溶けにくい物質を細胞内に留めておくことは困難です。そのため、これらの成分は細胞外へと排出されることになります。外部から見ると、それが滲み出てくるため、分泌されているように観察されます。
例えば、糖の分解の結果としてATPといったエネルギーが生み出されます。一方で、合成はエネルギーを消費する反応です。α酸およびその仲間は「軟樹脂画分」と呼ばれ、毬花あたり10~30%(商業生産されているホップ品種における値で、水分10%を含む乾物当たり)にも相当します(Biendlら、2014)。つまり、ホップの細胞は大きなエネルギーコストを払いながら、最終産物を細胞外へ排出し、分泌物を作り出していることになります。これらの分泌物は、ホップを取り巻く外部環境に対して、何らかのメッセージ性や働きかけの意味を持っていると考えられます。
α酸を貯蔵するルプリンの役割
ここまで、ルプリンには組織局在性があること、そして外部環境に対して何らかの役割を果たしているのではないかという、二つの考察を行ってきました。
実のところ、ホップにとってルプリンが果たす本来の役割は、まだ明らかになっていません。いくつかの仮説は存在します。たとえば、種子を鳥や昆虫による食害から守るため、あるいは病原菌の感染から守るため、といった説です(Biendl and Pinzl, 2008)。しかし、これらの仮説が実際に検証された例はないようです。
仮説を実証するためには、ルプリンを持たないホップを遺伝的に作り出し、通常のホップと比較する必要がありますが、それには多大な労力と時間がかかるため、現実的には誰も取り組んでいないのが実情です。そして仮にその役割が分かったとしても、「それが分かって何になるのか?」というのが正直なところかもしれません。
とはいえ、これまでに明らかになっている事実をもとに、矛盾の少ない仮説を構築することは有意義ですし、ホップの専門家を名乗る以上、避けられない問いでもあります。そこで私見として、ひとつの考察をまとめてみました。
ホップはビールの原料として広く知られていますが、古くから薬草としても利用されてきました。近年では、高感度な分析技術や培養細胞を用いた検証手法の進展によって、ホップに含まれる多様な成分がさまざまな効果・効能を持つことが明らかになってきています(Biendl and Pinzl, 2008)。健康機能性については第6章で詳しく述べますが、ここでは「抗菌性」に注目します。なぜなら、これまで述べてきたルプリンの役割を考える上で、ホップにとってもビールにとっても、抗菌性は極めて都合のよい説明となるからです。
ホップの抗菌性
ホップが食品の保存性を高めることは中世の頃から知られており、微生物、特にグラム陽性菌に対して強い増殖抑制効果があることが確認されています(Biendlら、2014)。ビールにおいては、IPA(India Pale Ale)がその代表的な例です。
18世紀末、インドを植民地としていたイギリスは、本国からインドへビールを輸送していました。赤道を2度越える航路を通り、到着までには5~6カ月を要したといわれています(富江、2019)。木樽に詰められたビールが、当時どのような味になっていたのかは想像を絶します。
微生物や殺菌といった概念がまだ存在しなかったこの時代、ホップを大量に加えることで品質が保たれることが経験的に分かり、その結果としてIPAが生まれたのです。
話はさらにさかのぼります。1516年、現在のドイツにあたる地域で「ビール純粋令」が発布されました。当時バイエルン地方を治めていたヴィルヘルム4世によって定められたこの法律では、「ビールの製造には大麦、水、そしてホップを使用すること」と定義されています。背景には政治・経済が複雑に絡んでいそうですが、品質面ではホップの抗菌性が大きく関係していたようです(Biendlら、2014)。
このようにビールの歴史を振り返ると、ホップが今日までビール造りにおいて欠かせない原料となった背景には、苦味や香りといった風味だけでなく、抗菌性によって保存性を高められるという点も見逃せない要素であったことが分かります。むしろ、この保存性がビールの広域流通を可能にし、市場の拡大・普及に大きく貢献した、真の役割に思えてなりません。
では、もし抗菌性がルプリンの役割であるとするならば、ホップにとってそれはどのような意味を持つのでしょうか。
ルプリンは種子の周囲に配置されていると述べましたが、これは、種子を微生物などの外敵から守るためなのかもしれません。毬花は秋までそのままにしておくと自然に崩れ、風にあおられると苞が花びらのように舞いながら地面に落ちていきます。もし種子がついていれば、内苞が種子を抱えたままです。内苞が羽根のように風を受け、より遠方に種子を運んでいるようにも見えます。土に落ちた内苞と種子は雨風にさらされながら、地面へ潜っていきます。このとき、ルプリンに含まれるα酸が水分によって溶け出し、種子の周囲の環境を衛生的に保ち、翌年の春に健全な発芽や初期生育を促しているのではないでしょうか。
私自身、ホップの品種改良において交配種子をひとつずつ丁寧に採種・播種する経験をしてきました。採種の際には、種子を毬花や苞から分離し、翌春にビニールハウス内で温度・水分管理を行いながら播種します。このとき、苗床には必ず蒸気で殺菌処理を施した土を使用するよう、師匠から教わりました。そして、3〜4cmほど成長した苗を露地圃場に定植するのです。
師匠が定年退職した後、試しに圃場へ直播してみたことがあります。しかし、発芽したのはごくわずかで、ハウス内の10分の1程度でした。温度や水分の管理だけでは不十分で、ホップの種子には衛生的な環境が不可欠であると改めて実感しました。そう考えると、種子周辺の衛生環境を保つためにルプリンが存在しているのではないか、という仮説が浮かびます。
これらはあくまでも現時点では未検証の仮説にすぎませんが、簡単な実験によって確認できるはずです。結果はいずれ公開したいと思いますが、少なくとも抗菌性というひとつの要素から、さまざまな周辺の事実と矛盾しない、もっともらしいストーリーが組み立てられました。都合のよい事実を並べただけと思われるかもしれませんが、筋の通った、意義のある仮説ではないかと感じています。
抗菌性のメカニズム
ホップの抗菌性については、特にビールにおけるメカニズムに関して多くの報告があります。ここでは、α酸に限らず、ホップ由来の苦味成分全体について説明いたします。
ビール製造において、微生物汚染は大敵のひとつです。もっとも、食中毒菌のような微生物はビール中では生存できないため、健康被害の原因となることはありません。ビールの環境、具体的には酸性、エタノール、炭酸ガス、そしてホップ成分の存在と嫌気状態が食中毒菌を殺菌してしまいます。
しかし、問題となるのは、ビールの風味を著しく損なう「ビール混濁菌(beer spoilage microorganisms)」です。代表的なものとしては、乳酸菌の一種である Lactobacillus brevis が挙げられます。この菌はビール環境にある程度適応しており、瓶や缶に充填された後でも増殖することがあります。その結果生じる風味劣化は、実に深刻です。世界中で確認されており、その脅威から多くの研究が行われてきました。
ホップの苦味成分は、一定以上の濃度になるとこのような細菌の増殖を抑制することが知られており、そのメカニズムについてもいくつかの説が提唱されています(Biendlら、2014)。
ひとつは「イオノフォア(Ionophores)説」で、苦味成分が細菌の細胞膜の透過性を変化させ、水素イオンを細胞内へ流入させるというものです(Simpson, 1993)。その結果、細胞内のpH(※ノート1-2)が低下し、生理的代謝に異常が生じ、正常な生育が困難になります(鈴木、2014)。もうひとつは、ホップ由来の苦味成分が細菌の細胞膜を酸化させ、その性質を変化させるというメカニズムです(Behr and Vogel, 2010)。この他にも多数の研究が存在しますが、筆者自身も別の視点から抗菌メカニズムを調べてみました。具体的には、細菌の生命維持に重要な代謝系の挙動を確認したところ、ある異常が見つかりました。これは有力な証拠になると考えましたが、関連する別の代謝系への影響が予想通りに見られず、仮説は崩れ、発表には至りませんでした。
このように、ホップの抗菌性のメカニズムは単一の現象ではなく、複数の作用が同時に関与していると考えられます。つまり、複数の代謝系に影響を及ぼす、複雑な作用機構を持っているのです。
ホップの苦味成分が抗菌作用を示す対象は、一般にグラム染色で紫色に染まる「グラム陽性菌」とされています(Biendlら、2014)。これらの菌に対しては、苦味成分が強い増殖抑制効果を示すことが確認されています。
一方で、グラム陰性菌は外膜構造の違いから、苦味成分を取り込めないとされ、抗菌効果がないと考えられてきました。しかし、グラム陰性菌の中にもビールを変敗させる細菌が存在します。もしかしたら効果があるのでは?という期待のもとで実験を行った結果、意外にも有効であることが分かりました。
グラム陰性菌のPectinatus frisingensis で試してみたのですが(尾形智夫 1999)、α酸に限らずS-フラクション、イソα酸(後述)の苦味成分それぞれで増殖が抑制され、またそれぞれを組み合わせると相加的な増殖抑制効果が確認できました(特許文献:特許第5864097~5864099号)。後にPectinatus菌は薬剤耐性試験からグラム陽性菌の性質を併せ持つこと、DNA塩基配列の比較からグラム陽性菌にも近いことが分かったようです。苦味成分への反応性がグラム陽性菌と共通していたのです。想定外の結果ではありましたが、非常に興味深い知見です。
ホップの抗菌性は、ビール製造にとどまらず、工業的な工程でも応用されています(Biendlら、2014)。たとえば、砂糖製造やバイオエタノール製造において、雑菌の増殖抑制に利用されています。ここで活躍しているのは、β酸です。
β酸は「triprenylated derivative of phloroglucinol」と呼ばれる構造を持ち、3本の側鎖を有しています。α酸が2本の側鎖を持つのに対し、1本多い構造です(Biendlら、2014)。
実はこのβ酸、ビールにおいてはあまり活用されていません。というのも、β酸はビール中にはほとんど残らない成分だからです(※ノート1-3)。その一方で、ホップ加工品の製造が進んでいる業界では、α酸を抽出する工程で副産物としてβ酸を多く含む残渣が発生します。現在では、この副産物を再利用し、天然の抗菌剤として活用する取り組みも進められています。
ホップの苦味成分たち
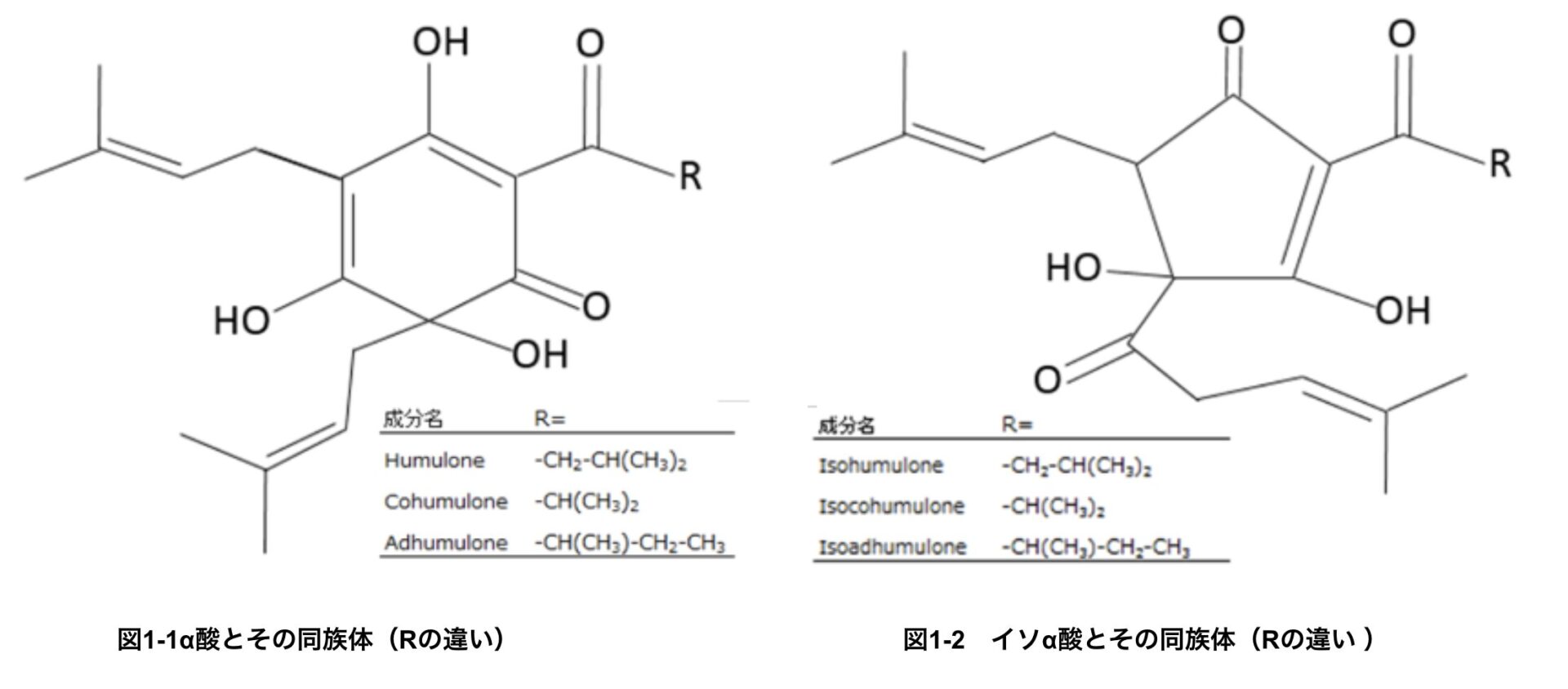
ビールの苦味の正体はイソα酸です。α酸と分子量は変わらないですが、六角形のα酸の構造(図1-1)が変化し、五角形のイソα酸になります(図1-2)。α酸からイソα酸へ構造が変化することを「異性化」と呼びます。α酸の異性化は熱によって起こります。ビール製造工程の麦汁煮沸時にホップを加え、よく煮てあげるとイソα酸は増えるのです。イソα酸への異性化は低温でも起こるようですが(岸本2021)、筆者の経験では80℃超えると急増します。
麦汁のpHが低い場合や糖度が高い場合は、異性化を抑える傾向にあります。どの程度の苦味になったかを知るには、苦味価、単位はBU(Bitterness Unitの略)を求めることですが、イソオクタンという有機溶媒を使ったこの分析法は、「苦味価=苦味の強度」と単純に解釈できない場合もあります(後述)。
イソα酸については、ほとんどの教科書や解説書に記載されていますが、実際にはビールの苦味はイソα酸だけによって生じているわけではありません。以下では、より多様な苦味成分についてご紹介します。
これまで何度も登場してきたα酸ですが、実はα酸は単一の成分ではなく、複数の類縁体からなる「α酸群」です。図1-1に示した構造中に「–R」と表記された部分があり、ここに何が入るかによって化合物の名称が変わります。
Biendlら(2014)によれば、Rには炭化水素の側鎖が付き、その炭素数や構造の違いによって、6種類に分類されます。代表的なものとして、フムロン(humulone)、コフムロン(cohumulone)、アドフムロン(adhumulone)があり、さらにポストフムロン(posthumulone)、プレフムロン(pre-humulone)、アドプレフムロン(adpre-humulone)などがあります。
筆者が研究現場にいた頃は、最初の3成分を中心に分析していましたが、後者3成分については分析の経験がなく、やや特殊な分析法が必要なのかもしれません。
以降、文章中で「α酸」と記す場合は、前述の主要3成分(humulone、cohumulone、adhumulone)を指すものとお考えください。これらを区別せずにまとめて言及する際には「humulones」と複数形で表記することもあります。
これらのα酸が異性化すると、名前の先頭に「iso-」が付加されます。たとえば、humuloneが異性化したものは「iso-humulone」となります。したがって、イソα酸とは、代表的にはこのような3種類の成分の集合と捉えることができます。
同様に、β酸も6種類に命名されていますが、α酸と同様、代表的な3成分としてはルプロン(lupulone)、コルプロン(colupulone)、アドルプロン(adlupulone)があり、これらを総称して「lupulones」と呼びます(図1-3)。
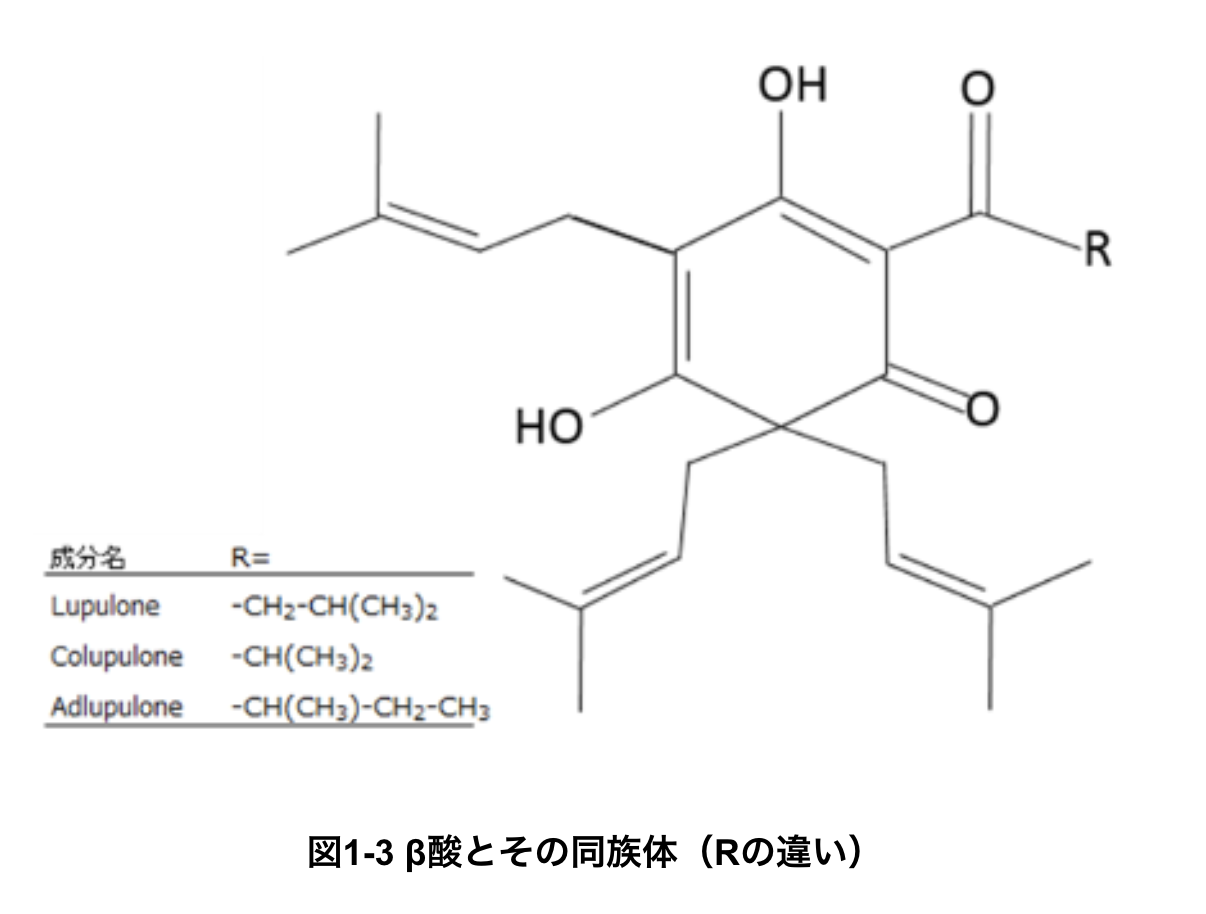
β酸は麦汁煮沸中に異性化せずに酸化します。ただし全てではなく約20%が酸化し親水性が増します(Biendlら2014)。酸化されたβ酸は名前が変わってhuluponesとなります。
ここからは、イソα酸の詳細について少し触れていきます。
ビール中の苦味の約70%は、イソα酸が寄与しているとされています(Biendlら、2014)。しかし、重要なのはイソα酸を構成する成分の内訳、特にiso-humuloneとiso-cohumuloneの割合です。この割合は、もともとのホップ品種に由来します。α酸を構成する各成分の割合(=α酸中に各成分が何%含まれているか)は、品種によって異なります。特にadhumuloneは品種による違いがあまり見られませんが、humuloneとcohumuloneの割合は品種ごとに大きく異なります。たとえば、cohumuloneが全α酸中の10%台の品種もあれば、50%近くを占める品種も存在します。その分、humuloneの割合はそれに応じて増減します。そして、煮沸によってα酸が異性化されても、イソα酸中の各成分の割合には元のホップ品種の特性が反映されるのです。
Cohumulone 論争
ビールの苦味の“質”について、いわゆる「Cohumulone論争」があります。
ビール中に含まれるイソα酸のうち、iso-humulone と iso-cohumulone の割合はホップの品種によって異なり、それによって苦味の質も変わるのではないかという議論です。
1991年、筆者が初めて参加したアメリカのビール学会でもこの話題が取り上げられており、「iso-cohumulone が多いと、苦味が鋭く収れん味を帯びるため好ましくない」とする立場と、「iso-cohumulone にそのような特徴は見られない」とする立場が真っ向から対立していました。
Peacock(2011)によれば、多くの検証(おそらくは異なるホップ品種で醸造したビール同士の比較)がなされたものの、「好ましくない」という評価が多かったようです。双方の主張については、Nickerson(1986)、Kapplerら(2010)、Peacock(2011)などの論文で紹介されています。さらに、iso-cohumulone のみを分離し、その味を直接評価する試みも行われています(Hughes and Simpson, 1996;Hughes, 2000)。しかし、Biendlら(2014)によると、現在に至るまでこの論争には明確な決着はついていないようです。
筆者の個人的な経験としても、iso-cohumulone の含有量が高いホップ品種で醸造したビールは、苦味が粗く、時に「辛い」と感じられることがありました。代表的な高 cohumulone 品種としては、Cluster や Bullion があり、これらは cohumulone 含有比が35~50%に達します。日本のホップ品種である IBUKI(旧:キリン2号)も40%台と高い数値です。IBUKIのみを用いて、苦味価30以上のビールを試作した際には、その粗さが明確に感じられました。一方で、苦味価を20程度に抑えた場合は、あまり気になりませんでした。
一方、チェコのBudvarが造るピルスナーは、チェコのSaazというホップを大量に使用しており、苦味価は30以上と思われますが、非常に心地よい苦味で、粗さはまったく感じられませんでした。現地工場の実験室で、新鮮な状態のビールを試飲した体験ですが、非常に印象的でした。Saazは cohumulone 含有率が20%前半と低い品種です。
こうした例から見ると、「iso-cohumulone が高い=心地の良い苦味ではない」という印象を受けるかもしれませんが、単純に結論づけるのは早計です。1970年代に始まったこの論争が、未だに結論に至っていないのには、それなりの理由があるはずです。
結論が出ていないにもかかわらず、ホップ育種の現場では、この論争が今なお大きな影響力を持っています。詳細については、後述する「ホップの育種」に関する章をご参照ください。
β酸が酸化して生成される hulupones は、少なからず苦味を持ち、その苦味は柔らかく、厚みのある印象を与えるとされています。一方、イソα酸は強く鋭い苦味を持つことで知られています。イソα酸は、単体では「Iso-extract」という水溶性のホップ加工品として入手することが可能です。筆者は、これを用いて、ホップを極少量しか使用していない苦味価の低いビールに添加してみました。
その結果、確かに明確な苦味は感じられましたが、苦味が消えていくとともに喉の奥にじりじりとした不快感が残り、全体としては「苦いだけで物足りない」という印象でした。単調でしつこく、決して心地よい苦味とは言えませんでした。
対照的に、先述のBudvarのビールでは、苦味がふんわりと立ち上がり、しっかりと感じられる一方で、すーっと引いていくような余韻がありました。その余韻は複雑で、まるでリズムを刻むように時間とともに異なる表情を見せてくれました。
イソα酸は確かにビールの苦味本体ですが、イソα酸に加え脇役が必要なのです。そのひとつがhuluponesなのです。次項では脇役たちについて解説します。
苦味成分の脇役たち
苦味の脇役を演じる成分があることは、以前より知られていました。しかし、これらの成分は微量であり、かつ多数が関与しているため、具体的にどの成分がどのように苦味に寄与しているのかについては、いまだ明確には解明されていません。
とはいえ、経験的には、これらの成分が明らかにビールの苦味に影響を与えていることが分かっています。
図1-4には、ビール中の苦味成分を高速液体クロマトグラフィー(HPLC)という分析装置を用いて測定した結果を示しています。
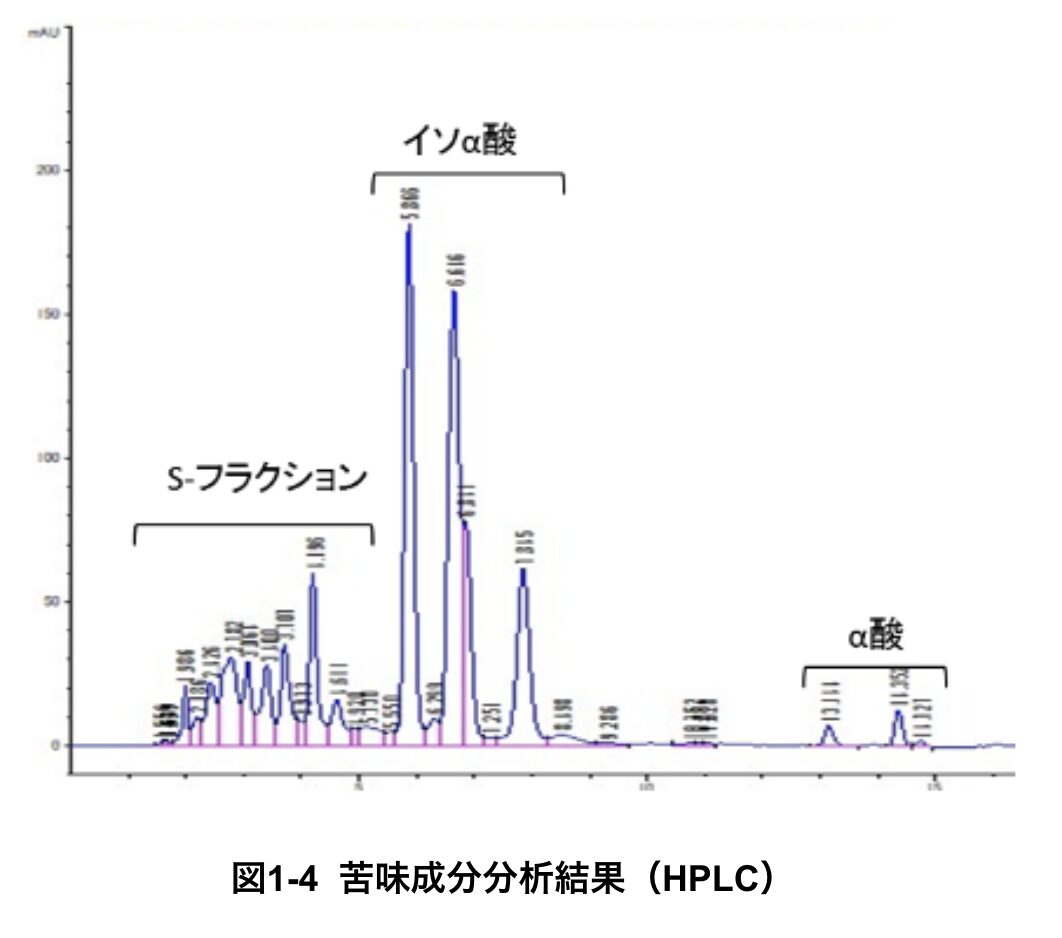
イソα酸は3つのピークとして検出され、左から順に iso-cohumulone、iso-humulone、iso-adhumulone に対応しています。検出される成分の極性(※ノート1-2)は、左ほど高く、右にいくほど低くなります。
苦味の脇役とされる成分は、このイソα酸の左側に検出される、より高い極性を持つ微量成分の集まりです。これらは、小若らによって NIBC(Non iso-humulone bitter compounds)、小野らによって S-フラクション(小野, 1999)、岸本(2021)によって OPC(Oxidative Polar Compounds)などと呼ばれています。本稿では、以後この成分群を「S-フラクション」と呼ぶことにします。
かつて、ホップは収穫後に麻袋で保管されていましたが、当時は現在のようにペレット化され密閉されているわけではなく、保管中にホップ成分は酸化されていきました。S-フラクションは、α酸やβ酸が酸化されて生成された成分群です。酸化が過度に進行すると、チーズ様や汗のような不快な香りを放つ物質に分解されてしまいますが、適度な酸化はむしろ、質の良い苦味をもたらすことが知られています(特許第5832739号、特開2011-139671号)。
酸化の進行度合いはHPLCによる分析で把握できます。S-フラクションの増加量と、α酸・β酸の減少量を定量することで、おおよその酸化状態がわかります。ただし、S-フラクションの中身は、humulones や lupulones の酸化物から生じた多数の微量成分で構成されており、その詳細な把握には高感度かつ高分解能の分析技術が必要です。
Taniguchiら(2015)は、非常に高度な分析技術と根気強い取り組みにより、S-フラクションに含まれる多数の成分の同定・定量に成功しました。具体的には、humulinones、4′-hydroxyallo-humulinone、tricyclooxyisohumulones、β酸由来の hulupones などが確認されており、それぞれ酸化様式や立体構造の変化によって多様な特性を示します。これらの酸化成分は極性が高いため、ビール中に溶けやすく、味にも寄与します。
後熟条件を変えて酸化の程度を調整したホップや、水溶性の高さを利用してS-フラクションのみを抽出した画分などを用いて、実際にさまざまなビールを醸造してみました。その結果、S-フラクションを加えることで苦味の質が明らかに温和になり、苦味に加えてコクのある余韻も感じられるようになりました。ただし、S-フラクションだけでは不快な味になることもわかりました。
具体的には、飲んだ直後に少し遅れて渋みが立ち上がり、そのまま長く続く、メリハリのない味わいとなってしまいました。このことから、S-フラクションはイソα酸と共存することでその効果を発揮することがわかります。つまり、イソα酸が主役だとすれば、S-フラクションはその魅力を引き立てる名脇役といえるでしょう。
S-フラクションの量は、ホップの後熟だけでなく、ビールの仕込み工程においてもある程度調整が可能です。S-フラクションはおよそ70℃程度で抽出されやすくなり、煮沸によって減少することが確認されています(特許第5832739号、特開2011-139671号)。
このS-フラクションを意図的に増やしたビールを試作し、官能評価では狙い通りの結果が得られました。さらに興味本位で「味センサー」と呼ばれる機器でも測定してみました。この装置は複数のセンサーを備えており、味の要素を数値化することができます(特開2011-139671号)。
その結果、S-フラクションを増やすことで苦味、渋み、後苦味の信号が予想通り低下しました。一方で、予想外だったのは塩味センサーが強く反応したことです。このセンサーは本来、食塩(NaCl)に反応する設計ですが、S-フラクションが塩味として反応した可能性が示唆されました。
この結果から、S-フラクションは苦味の受容体へのイソα酸の結合を妨げ、苦味ではなく“塩味”として感じられる影響を与えている可能性があります。では、いったい何が起こっているのでしょうか?
人間は、舌や口腔内に存在する味細胞で五味(甘味、酸味、塩味、苦味、旨味)を検知しています。これらの味細胞には、それぞれの味に対応する受容体が存在しており、苦味・甘味・旨味はGタンパク質共役型受容体、塩味・酸味はイオンチャネル型受容体で認識されています。また、苦味の受容体は T2Rファミリーと呼ばれ、現在までに26種類が知られています。
分子レベルでの味の受容メカニズムには不明な点も多いものの、日常生活の中で五味の相互作用を私たちは経験的に理解しています。たとえば、かつお節や昆布の「だし」の旨味が塩味を引き立てる現象や、スイカやトマトに塩を振ることで甘味が際立つ例などです。
この現象の脳科学的な解明は最近の事のようです。甘味受容体の細胞にはトランスポーターという運び屋も居て、この運び屋は甘味成分と塩味成分が共存すると甘味成分を積極的に甘味受容体に結合させるようです(Yasumatsuら2020)。そのため塩味存在下では甘味の成分の受容体への結合が促進され、甘味を強く感じるのです。
また、複数の味成分が同時に作用すると、受容体の立体構造(3次構造)そのものが変化し、味の感じ方に影響を与えるという報告もあります。相互作用は、味のシグナルを受け取る1次反応の変化が本質のようです。
今後の研究が待ち遠しい分野ですが、S-フラクションの作用機作もいずれ解明されることを期待します。
ビールでのホップの苦味についてもうひとつ、関連した現象を紹介しましょう。
フルーツビールの教え
フルーツビールを作ってみました。「果汁を加えれば簡単にできるだろう」と安易に考え、通常のビールに果汁を混ぜてみたのです。しかし、これがひどく不味いものでした。味はバラバラで、特に苦味の質が大きく変わり、いがらっぽく鋭い苦味に加えて、渋みも感じられました。
なぜこのような変化が起こるのかを探っていく中で、たどり着いたのが「有機酸」でした。有機酸は文字通り酸味をもつ成分で、どうやら苦味の質との相性に関係があるようです。有機酸にはさまざまな種類がありますが、ここでは代表的なクエン酸、リンゴ酸、酒石酸の3種に絞って説明します。
通常のビールでは、クエン酸は麦芽から、リンゴ酸は酵母の代謝によってある程度生成されますが、酒石酸は基本的に生成されません。しかし、フルーツビールでは果汁を加えることで、有機酸の含有量が大きく増加します。
そこで、各有機酸を少量ずつ添加し、苦味の質に与える影響を検証してみました。単独での添加だけでなく、複数を混合した場合でも、苦味に影響を与える「上限」が存在することが分かりました(特許文献:特許第6727974号、特開2019-165709、特開2019-165710、特開2019-110844、特開2019-110843)。
感覚的には、苦味との相性は「クエン酸 > リンゴ酸 > 酒石酸」の順であり、この上限を超えると苦味価を下げる以外に方法がありません。
なお、果物の種類によって含まれる有機酸の種類が異なるため、苦味への影響は単純に予測できません。参考までに、果物ごとの主な有機酸の特徴を以下にまとめます。
- クエン酸が多い:グレープフルーツ、ユズ、スダチ、日向夏などの柑橘類
- リンゴ酸が多い:リンゴ、モモ、チェリー、スイカ
- クエン酸とリンゴ酸が多い:パイナップル、イチジク、バナナ
- 酒石酸が多い:ブドウ、青梅
次に、有機酸がどのようにして苦味の質に影響を与えるのかについて考えてみます。有機酸が加わることで、ビールのpHが低下し、それが苦味質に影響を及ぼすと考えられます。
クエン酸、リンゴ酸、酒石酸のpKa値(※ノート1-3)はおおよそ3付近で、ビールのpH(通常4程度)よりも低いため、ビール中でこれらは解離し、水素イオンを放出してpHを下げます。
イソα酸は、pHが低下すると非解離型が増える性質を持ちます。もし、非解離型イソα酸の苦味の質が「悪い」とするならば、このpH変化による味の変化ともつじつまが合います(※この点はSchönberger, 2009 の記述とは異なりますが)。
ビールには緩衝能と呼ばれるpHの変化を吸収する性質があるのですが、pHが下がるにせよ極端な変化ではなく微減程度の範囲でしょう。微妙な変化なら影響は少ないと感じられるかもしれませんが、実はビールの味はpHが0.1変わっただけでも明らかな違いと感じることができます。したがって、有機酸によるpH低下が苦味質に与える影響は、十分にあり得ると考えられます。
今回、有機酸と苦味の関係を調べる中で、フルーツビールの作り手たちが経験してきたであろう試行錯誤や苦労、そして工夫の積み重ねに思いを馳せることができました。まさか、ホップの「苦味の質」がそのきっかけになるとは思いもよりませんでした。
改めて、ビールという飲み物は実に奥深く、懐の深い世界だと実感しました。フルーツビールは決して「果汁を入れればできる」といった単純なものではなく、絶妙なバランス感覚と、それを形にする技術を持った作り手がいてこそ完成するものなのです。
苦味価とは
ときどき、苦味価(BU)が50、60、あるいはそれ以上であることをうたったクラフトビールを目にすることがあります。本章では苦味について扱っていますので、この「苦味価」についても解説したいと思います。
一般的なビールの苦味価は20程度です。したがって、苦味価60のビールは理論上その3倍も苦いということになります。しかし実際に飲んでみると、意外と普通の苦味で、驚くような強さではないことが多いのです(もちろん、中には驚くほど苦いビールも存在します)。
苦味価は官能的な苦味の強さと相関するものとして、世界中で採用されている指標ですが、なぜこのような乖離が生まれるのかを説明します。
まず、分析方法について簡単にご紹介します(※ノート1-4)。
最初に苦味成分の抽出工程です。一定量のビールに塩酸を加えてpHを1まで下げます。そこに有機溶媒であるイソオクタンを加え、激しく攪拌・振とうさせた後、静置してビールとイソオクタンの2層に分離させます。
次に測定工程です。イソオクタン層の一部を回収し、275nmの紫外線を照射し、吸収された光の強さを測定します。この吸収値に50を掛けたものが苦味価(BU)となります。
この方法は比較的簡便で、特別な器具は吸光度計程度で済むため、古くから広く使われてきた分析法です。
しかし、この方法では「苦味成分だけ」を測定しているわけではありません。
特に、苦味価が異常に高く表示されるケースでは、色度の高い黒ビールが多い傾向にあります。その理由を説明します。
イソオクタンは炭素と水素のみから成る、非常に極性の低い有機溶媒です。水を主成分とするビールとは混ざり合わず、2層に分離する性質があります。
抽出時にpHを1にするのは、苦味成分などが持つ -O⁻ や -COO⁻ といった解離状態を、非解離の -OH や -COOH の形に戻すためです。イソα酸も非解離状態になることで極性が下がり、イソオクタンに溶けやすくなります。イソα酸は275nm付近の紫外線をよく吸収するため、その吸収の程度を苦味価に換算しているわけです。
つまり、この分析は「イソα酸を測定している」のではなく、「酸性下でイソオクタンに溶け、275nmの紫外線を吸収する成分全体を測定している」ことになります。その中にイソα酸が含まれている、という構図です。
黒ビールで苦味価が正確に測定できないのは、色素が混入してしまうからです。ビールの色は麦芽に由来し、製麦中の麦芽の加熱工程で起こる反応によって色素は生まれます。加熱工程ではカラメル反応(糖と糖の反応)、メイラード反応(糖とアミノ酸の反応)により低分子から高分子の成分が作られます。生成物が多様過ぎて未だに全容がつかめていない反応ですが、その中で可視光を吸収するのが色素なのです。ビールの色素は、メイラード反応産物で高分子のメラノイジンが主ですがイソオクタン層に溶けません。イソオクタン層は染まらないのです。
混入して苦味価を上昇させる成分として、低色素で低分子な成分が想定されるわけですが、そのような成分としてperlolyrineが見つかりました(村田2019)。しかも275nmに最大吸収を示し黒ビールに多めに含まれていました。構造式を見た限り疎水性部分が多く酸性下ではイソオクタンに溶け込みそうです。この成分はメイラード反応によって生成された多種多様な成分たちのひとつです。似たような成分が沢山あるのでしょう。その様な成分が苦味価として測定されてしまったのです。
苦味価に影響を与えるもう一つの例として、ドライホッピングを取り上げてみましょう。
ドライホッピングでは、ホップは低温の貯蔵工程において添加されます。加熱を伴わないため、α酸はイソα酸に異性化されず、苦味の主成分であるイソα酸は増加しません。しかしながら、ホップ由来のS-フラクションやα酸そのものがビール中に溶解し、それらも275nmの紫外線を吸収するため、結果として苦味価には反映されます。
そのため、ドライホッピングを行ったビールでは、実際の苦味の体感とは異なり、苦味価が高めに測定される傾向があります。このように、苦味価の数値だけでは苦味の強さや質を正確に判断することはできません。ビールの製法や使用されたホップの処理方法なども、あわせて考慮する必要があるのです。
ノート 1-1 毬花
ホップの「毬花」は、「球花」とも書き、「きゅうか」と読みます。英語では Hop cones と呼ばれています。
近年では、「毬花」の漢字表記から「まりばな」と読む場合も見られます。
「花」という字が使われているため、いわゆる“花”を連想しがちですが、生物学的には通常の花ではなく、「変形花」と呼ばれる構造に分類されます。毬花は、一見すると複数の花びら(花弁)から構成されているように見えますが、実際には花弁ではなく、葉が変形したもの、あるいはアジサイのように「がく」に相当する構造と考えられています。
それでは、ホップの“本来の花”はどのようなものかというと、毬花が形成される約1カ月前に現れます。とはいえ、この花も花弁を持つわけではありません。数十本の白い雌しべが一斉に伸びた状態で現れ、これは「毛花(けばな)」と呼ばれています(詳細は「育種」の章をご参照ください)。
ホップは風媒花であり、受粉のために雄株から風によって運ばれてくる花粉を待っています。そのため、昆虫の訪問を期待していません。したがって、色鮮やかな花びらや甘い蜜を持たないのです。
ノート 1-2 pH
pHとは、水素イオンH+と水酸基イオンOH-のバランスです。水素イオンが多いほどpHは低くなります。水酸基イオンは逆になります。ビールのpHは普通4前後ですが、製造工程で段階的にpHは下がってきます。
お湯は中性(pH7、水素イオンと水酸基イオンは等量)ですが粉砕した麦芽を溶かすと酸性成分によってpHは下がります。次に麦芽のたんぱく分解酵素とでんぷん分解酵素が働き、麦汁が出来上がり、この時のpHは5を少し上回る程度です。酵母が加わり発酵が始まるとさらにpHは下がっていきます。発酵では酵母の呼吸やアルコール発酵等、様々なことが起こりますが(そのため一言では説明し難いのです)、水素イオンと水酸基イオンの比率が一定方向(pHが下がる方向)に変化し最終的にpH4程度になる比率に落ち着きます。
ノート 1-3 成分の性質
ある成分の性質として、極性高い、低いとか疎水性、親水性と言ったりします。これらを水に対する溶解性として説明してみることにします。
油と水は混じりません。これは油と水では異なる性質だからです。水はH2Oですが、酸素Oに水素Hの電子が引っ張られて+(プラス)と‐(マイナス)の傾きが生じます。これが、極性が高い状態です。一方、油は炭化水素(CとH)が何度も結合した長い鎖のような構造を持ちます。例えばCH3-CH2-CH2-(繰り返し)の部分は、プラス、マイナスを持たない、極性が低い状態となります。
混じる、溶解するとは、同じ性質同士でなければなりませんので、極性の高い水と低い油は混じらないわけです。別章で扱う香りの成分(精油成分)のうちテルペンは炭化水素のみで構成され極性が低く、水には溶け難い疎水性の成分です。ここに-OHや-COOHが加わると性質は変わります。酸素OはCやHの元素の電子を引き付ける力が強く、成分全体で見るとマイナスに傾いている部分とプラスに傾いている部分を併せ持ち、傾きがある状態、極性がある状態になります。極性の程度に応じて疎水性が緩んだ分、親水性を持つことになります。電子を引き付ける力は、N(窒素)、P(リン)は強力です。
イオンに電離する、しないは、溶解した後の状態です。ある一つの成分がどの程度電離するかは、その成分が置かれたpH(水素イオン濃度)に依存します。-OHが-O–になる例で説明しますと、-O–はpH が下がってくると-OHの非電離状態に戻りますが、その程度は成分ごとに異なるのです。ホップのα酸、β酸の話に戻ると、電離、非電離は、解離という言葉に代わって(電離より広い意味になりますが、ここでは同じ意味です。)、酸解離定数pKa で記述される性質です。pKaは解離した分子と非解離分子が同量、1:1になるpH を示し、pKaから離れると解離・非解離の比率が急減、急増します。
α酸を構成するhumuloneのpKaは5付近、β酸のcolupuloneでは6付近です(水での値、Simpson, 1993b)。ビールのpHは4前後普通なので、α酸のうち10%が解離しますが、β酸では1%しか解離せず殆どが非解離した状態です。安定した溶解状態にはなく、やがて凝集や他の疎水性成分とくっついて沈殿してしまうでしょう。
しかし、非解離成分だから機能を発揮する場合もあります。細菌に対する抗菌作用です。細菌は疎水性の細胞膜で細胞内外を隔てていますが、外環境から様々な成分を取り込むためには、極性の低い成分でないと都合が悪いのです。疎水性の細胞膜が極性成分の進入を遮るからです。Simpson and Smith (1992)はpHを低くすると苦味成分の抗菌性がより高まることを示し、その理由は非解離成分が寄与している、と述べています。
ノート 1-4 分析法について
ビール業界では、原料を含む分析方法が世界的に統一されています。アメリカには American Society of Brewing Chemists(ASBC)、ヨーロッパには European Brewery Convention(EBC)という組織があり、いずれも大学、ビールメーカー、原料会社など、ビール関連業界の専門家によって構成されています。
これらの組織は定期的に学会を開催し、研究成果を発表し合っています。また、組織内には化学分析の専門家による「分析専門部会」が設けられており、各種分析方法はそこで標準化されています。
アメリカとヨーロッパで採用されている分析方法はほとんど同じですが、一部異なる場合もあります。そのような場合には、分析データにどちらの方法を用いたかを明記するのが通例です。
たとえば、ビールの色を測定する際には、使用する機器や換算方法に違いがあるため、「色度10EBC」などのように、単位とともに使用した基準を明記します。
引用文献
- Behr., J. B. and Vogel, R. F., Mechanisms of hop inhibition include the trancemembrane redox reaction, Appl. Environ. Microbiol.,76, 1, 142-149, 2010
- Biendl, M. and Pinzl, C., Hops and health. Botany, German hop museum Wolnzach, Germany, 2008
- Biendl, M., Engelhard, B., Foster, A., Gahr, A., Lutz, A., Mitter, W., Schmidt, R. and Schonberger, C., Hops Their cultivation, composition and usage, Fachverlag Hans Carl, Nuremberg, Germany, 2014
- Hughes, P. S. and Simpson, W. J., Bitterness of Congeners and Stereoisomers of Hop-Derived Bitter Acids Found in Beer, J. Am. Soc. Brew., 54, 4, 234-237, 1996
- Hughes, P., The Significance of Iso-α-Acids for Beer Quality Cambridge Prize Paper, J. Inst. Brew., 106, 5, 271-276, 2000
- Kappler, S., Krahl, M., Geissinger, C., Becker, T. and Krottenthaler, M., Degradation of Iso-α-Acids During Wort Boiling, J. Inst. Brew. 116, 4, 332-338, 2010
- Nickerson, G. B.,Williams, P. A. and Haunold, A., Varietal Differences in the Proportions of Cohumulone, Adhumulone, and Humulone in Hops, J. Am. Soc. Brew., 44, 2, 91-94, 1986
- Peacock, V., Percent co-humulone in hops: Effect on bitterness, utilization rate, foam enhancement and rate of beer staling, Master Brewers Association of the Americas conference, O-13, 2011
- Schönberger, C., Why cohumulone is better than its reputation, Brauwelt Int., 27, 3, 159-160, 2009
- Simpson, W. J. and Smith, A. R. W., Factors affecting antibacterial activity of hop compounds and their derivatives, J. Appl. Bacteriol., 72, 327-334, 1992
- Simpson, W. J., Ionophoric action of trans-isohumulone on Lactobacillus brevis, J. Gen. Biol.,139, 1041-1045, 1993 a
- Simpson, W. J., Ionization behavior of hop compounds and hop-derived compounds, J. Inst. Brew., 99, 317-326, 1993 b
- Taniguchi, Y., Matsuoka, Y., Taniguchi, H., Koizumi, H. and Katayama, M., Development of preparative and analytical methods of the hop bitter acid oxide fraction and chemical properties of its components, Biosci. Biotechnol. Biochem., 79, 10, 1684-1694, 2015
- Yasumatsu, K., Ohkuri, T., Yoshida, R., Iwata, S., Margoiskee, R. F. and Ninomiya, Y., Sodium-glucose cotransporter 1 as a sugar taste sensor in mouse tongue, Acta Physiol(oxf), 230, 4, 13529, 2020
- 尾形智夫,ビール有害菌の検出方法の進歩,醸造協会誌,94, 10, 786-791, 1999
- 小野美代子 醸造の成分,財団法人日本醸造協会,252-258,平成11年12月10日,1999
- 岸本徹.「苦味価」は何を語るか?, 醸造協会誌,118, 10, 688-697, 2021
- 鈴木康司, ビールを生息地として進化してきた乳酸菌たち,醸造協会誌,109, 8, 568-575, 2014
- 富江弘幸, 教養としてのビール, SBクリエイティブ株式会社, 東京, 2019
- 村田溶常, メイラード反応と着色・褐変 酸とアミノ酸が反応すると茶色くなる化学, 化学と生物, 57, 4, 213-220, 2019
- 特許文献:特開2011-139671 後熟ホップ様苦味を付与した発酵アルコール飲料
- 特許文献:特開2019-110843 果実由来のフルーツ香気と共存し、かつ、渋味の低減された発酵アルコール飲料の製法
- 特許文献:特開2019-110844 果実由来のフルーツ香気と共存し、かつ、渋味の低減された発酵アルコール飲料の製法
- 特許文献:特開2019-165709 果実由来のフルーツ香気と共存し、かつ、渋味の低減された発酵アルコール飲料の製法
- 特許文献:特開2019-165710 果実由来のフルーツ香気と共存し、かつ、渋味の低減された発酵アルコール飲料の製法
- 特許文献:特許第5832739号 後熟ホップ様苦味を呈する高芳醇発酵アルコール飲料
- 特許文献:特許第5864097号 ビール様飲料の製造方法
- 特許文献:特許第5864098号 ビール様飲料の製造方法
- 特許文献:特許第5864099号 ビール様飲料の製造方法
- 特許文献:特許第6727974号 発酵麦芽飲料およびその製造方法、ならびにホップ由来の苦味を有する発酵麦芽飲料に温和な苦味質を付与する方法
目次
はじめに
第1章 ホップの苦味の科学
・はじめに抗菌性あり!
・α酸を貯蔵するルプリンの役割
・ホップの抗菌性
・抗菌性のメカニズム
・ホップの苦味成分たち
・Cohumulone論争
・苦味成分の脇役たち
・フルーツビールの教え
・苦味価とは
・ノート1-1 毬花
・ノート1-2 pH
・ノート1-3 成分の性質
・ノ-ト1-4 分析法について
・引用文献
第2章 ホップの香りの科学
・香り成分分析技術の進歩のおかげ
・ホップとビールでの成分組成の違い
・ホップ香気成分の世界
・香気成分の間に起こる相互作用
・香りはどうように感知されるのか
・香気成分データの解析
・ホップ品種の香気のアイデンティティーはどの様に決まる?
・ノート2-1 テルペン類
・ノート2-2 濃度単位のお話し
・ノート2-3 含硫成分の分析
・ノート2-4 多変量解析
・引用文献
第3章 ホップ使用技術
・ビールの作り方
・苦味の付け方
・ホップ香気の付け方
・ホップの加工・調製品
・生ホップの特徴とは
・ルプリンパウダーの教え
・引用文献
第4章 ホップの育種
・交配育種の始まり
・雄ホップと交配育種
・遺伝の基礎
・ホップの遺伝学
・Cohumulone(Coh)論争の考察
・新ホップ品種MURAKAMI SEVENのいきさつ
・ホップ品種のアイデンティティーとは
・ホップのテロワール
・ノート4-1 遺伝学用語の解説
・ノート4-2 成分比率の実験系の補足
・引用文献
第5章 ホップの進化遺伝学
・分子進化遺伝学
・PCRの登場
・分子進化時計
・野生ホップ収集開始
・世界の野生ホップのDNA解析
・Humulus属の構成
・DNA塩基の違い
・ホップの起源の地
・分岐年代の推定
・ホップの伝播のシナリオ
・マイクロサテライトDNA多型
・コーカサス地方のホップ
・日本の野生ホップ
・日本野生ホップ、カラハナソウの分布
・カラハナソウと氷河期(最終氷期)との関係
・ノート5-1 分子進化時計のキャリブレーション
・ノート5-2 マイクロサテライトDNA多型
・ノート5-3 コーカサス集団とヨーロッパ集団の分岐年代推定
・引用文献
第6章 ホップを取り巻く環境の変化
・ビール事情の変化
・世界のホップ育種事情の変化
・世界のホップ生産事情の変化
・日本のホップ事情
・遠野、Now!
・ホップの新たな可能性-ホップの健康機能性-
・引用文献
付録:ホップの育て方
・成長のフェーズ
・ホップの育て方-作業-
・ホップの育て方-施肥-
・ホップの育て方-病虫害、自然発生被害-
・ホップの収穫
・ホップ栽培、あるある!
・将来のホップ栽培のために
・引用文献
おわりに
※校正しながら連載を進めますので、目次の一部が変更となる可能性があります
お知らせ
連載の更新情報は、GOOD HOPS公式SNS(X・Facebook)で随時お知らせします。
ぜひフォローしてチェックしてください。
X
facebook
また、村上が手がけたGOOD HOPSのビールも現在販売中です。下記のリンクよりご確認ください。
一般の方向けオンラインショップ
業務店さま向けオンラインショップ
お問い合わせ
施設やTAPROOMに関するご質問、自社ビールのお取り扱いに関するお問い合わせ(小売店様・飲食店様向け)、取材のご依頼など、どうぞお気軽にご連絡ください。
スタッフ一同、美味しいビールとともにお待ちしております!



